口服营养补充(oral nutritional supplement , ONS)除正常食物外,用特殊医学用途配方食品经口摄入以补充日常饮食不足的一种人工肠内营养治疗手段。ONS为各类急、慢性疾病患者提供普通自然饮食外的能量和营养素补充,例如普遍应用于慢性阻塞性肺疾病、艾滋病、慢性肾病、肿瘤等慢性消耗性疾病患者住院和居家环境中。根据国家卫生健康委员会2022年5月发布的《临床营养专业医疗质量控制指标(2022年版)》中明确的临床营养专业质控指标所涵盖的营养科工作量大体系之一,“营养风险筛查-营养评估-营养诊断-营养治疗”中的一体化营养诊疗流程中的营养治疗环节中应用最为广泛,见图1。
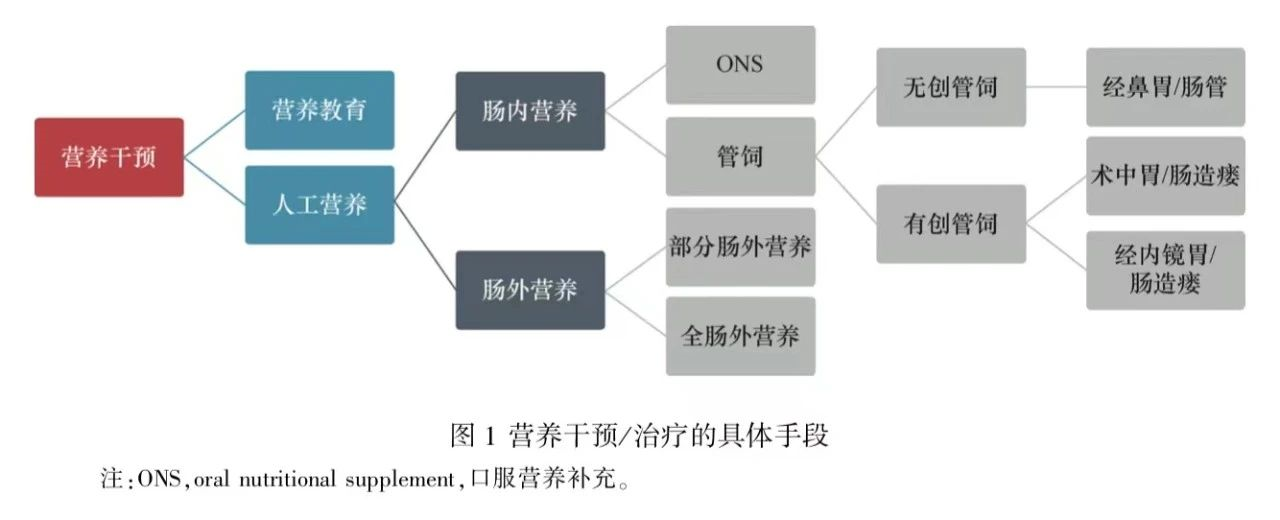
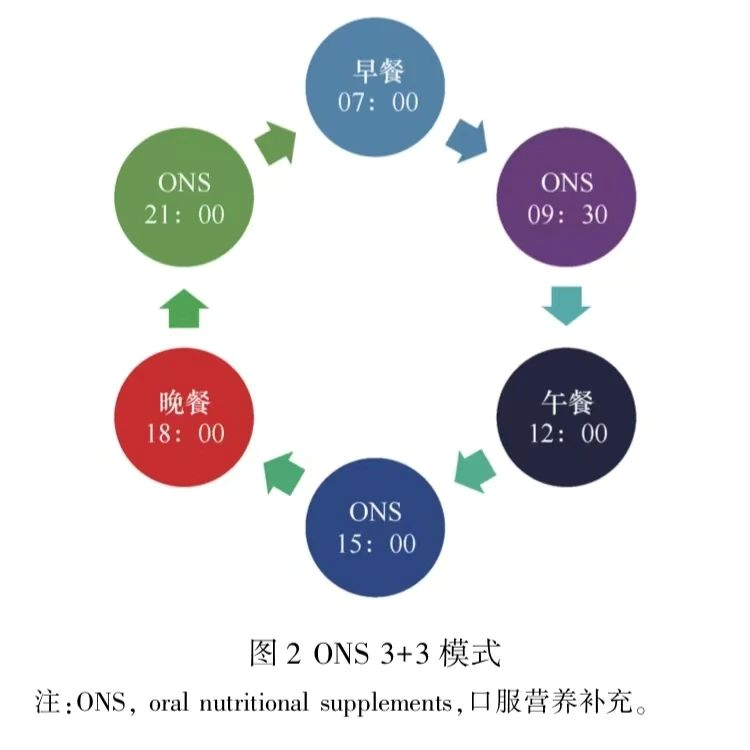
欧洲肠外肠内营养学会(European Society for Parenteral and Enteral Nutrition, ESPEN)于2006年至2022年发布的肿瘤肠内营养指南都认为在头/颈部和胃肠道放疗期间,饮食咨询和ONS可防止体重丢失和放疗中断,肿瘤患者如已存在营养不良或食物摄入明显减少超过7~10d,应开始包括ONS在内的肠内营养治疗。ONS制剂可以是肠内营养制剂、多元维生素和微量元素,甚至是鱼油、谷氨酰胺等药理性营养素。以肠内营养制剂而言,液体、半固体、粉状剂型最为常见,其宏量营养素比例均衡,能量密度在1.0~2.4kcal/ml或者kcal/g之间,可以根据容量大小包装为纸盒装、瓶装、袋装、软包装形式。ONS制剂营养素的类型和比例取决于实际应用场景的需求,在肿瘤患者适用的ONS剂型中,通常会考虑糖脂比例低(接近1∶1)、含有免疫增强型特殊营养制剂如鱼油等。LuZ等对328例胃食管癌患者进行随机对照试验发现,包括肿瘤科医师、护士、营养师、心理医师在内的早期多学科支持干预可以将受试者整体生存时间延长2.9个月(HR=0.68; 95%CI=0.51~0.90; P=0.021),研究组采用了营养风险筛查2002(nutritional risk screening 2002,NRS 2002)量表和患者主观全面评价(patient-generated subjective global assessment, PG-SGA)量表明确存在营养风险和营养不良,并针对筛查和评估结果进行干预。头颈部肿瘤控瘤治疗过程中最常见的不良反应是口腔黏膜炎,口服补充维生素 E、锌、谷氨酰胺对口腔黏膜炎的预防治疗具有一定效果。Martin B等分析了ONS对头颈部肿瘤患者的成本-效益,发现在平均6年的随访时间内,ONS组的生存率较单独营养咨询组要高。Gillis C等2018年报道了一项系统评价和meta分析,对914例接受结直肠手术患者的临床结局和机体功能进行分析,指出营养干预措施是手术患者预康复的关键组成部分,不论是单独的营养手段还是结合运动康复于一体的整合干预均会显著缩短结直肠手术后的住院时间。2021年,WobithM和Weimann A从加速康复外科(enhanced recovery after surgery, ERAS)的角度提出术前使用ONS至少7d可降低感染率等并发症,缩短住院时间。吴国豪团队2021年先后报道了2项随机对照试验结果,出院后居家用ONS可改善胃和结直肠手术患者的营养状况、肌肉质量、化疗耐受性和生活质量,特别强调改善肿瘤患者肌肉减少症的主要障碍在于缺乏意识和有效的训练支持,而ONS和身体锻炼在肿瘤患者肌肉减少症管理中潜力巨大。强化某些特殊营养底物的ONS如维生素D、β-羟基-β-甲基丁酸酯(β-hydroxy-β-methylbutyrate, HMB)和亮氨酸在一些研究中也被证实有很好的应用前景。Kim SH等对胰腺和胆管肿瘤进行化疗的患者使用ONS干预,发现8周后患者脂肪量增加,第1个化疗期结束后受试者的体重、去脂体重、骨骼肌、细胞量等均高于对照组,第2个化疗期结束后差异更加显著,与此同时,患者PG-SGA评分和生活质量评分30(quality of life questionnaire core 30,QLQ-C30)中疲劳评分在ONS组得到了改善。该研究使用的高能量密度配方(1.13kcal/ml) 给每例ONS的受试者提供能量400kcal/d,蛋白质19g/d。Faccio AA等在一项多中心、随机对照、开放标签研究中给放疗/放化疗患者包含乳清蛋白、亮氨酸和锌的ONS补充剂(计划给予量为前4d逐渐增加至630kcal,实际受试者的中位数日均摄入量为332kcal)+营养咨询,对照组为仅给予营养咨询,两组患者干预4周后在体重、去脂体重百分比等方面无统计学差异,而ONS的不良反应主要是恶心/呕吐、腹泻、便秘。Grupińska J等分析了ONS对接受术后辅助化疗的乳腺癌女性的身体成分和生化参数的影响进行了分析,经过6周化疗后,无论ONS组女性的年龄如何,其肌肉质量、去脂肪体重(fat free mass,FFM)和去脂肪体质指数(fat free mass index,FFMI)均较无ONS组显著增加,ONS组受试者的清蛋白水平、甘油三酯和高密度脂蛋白胆固醇水平均较对照组更为稳定。尽管ONS对于肿瘤患者特别是老年肿瘤患者的益处很多, 但也需要关注其他问题。Coffey N等报道口服营养补充剂的糖含量可能很高, 特别是粉状口服营养补充剂与200ml全脂牛奶混合后,每份含16.4~35.0g糖。虽然有助于患者保持健康的体质指数,但可能会增加患龋齿的风险。与此同时,口服营养补充剂应是预防和改善肿瘤手术患者营养问题的首选,但ONS如被过度使用或使用不当,也会导致许多临床疾病,且会增加医疗保健负担。非荷瘤生存者的营养治疗配方与良性疾病患者无明显不同,可首选标准配方特医食品或肠内营养剂;荷瘤状态下,配方应区别于良性疾病,推荐选择肿瘤特异性营养治疗配方。营养不良的诊断目前的依据是ESPEN2015诊断标准和全球领导人营养不良倡议(Global Leadership Initiative on Malnutrition, GLIM)。GLIM标准包括3个表型标准(非自主体重丢失、低BMI及肌肉减少)和2个病因标准(摄食减少或消化吸收障碍,炎症或疾病负担),具备1个表型标准和1个病因标准即可以诊断营养不良。GLIM“一步法”和NRS 2002-GLIM“两步法”对于营养不良诊断的一致性较好。从营养诊疗流程讲,ONS 应是在营养诊断成立后,在营养咨询/健康教育同时开展的一项人工营养治疗,但对于很多患者,特别是荷瘤患者,控瘤治疗无效后才进行营养治疗,往往为时已晚。因此,石汉平团队提出营养不仅成为肿瘤患者的基础治疗、一线治疗,而且应该早期启动且为全程、主动治疗手段。(1)肿瘤术前:中华医学会肠外肠内营养学分会(Chinese Society for Parenteral and Enteral Nutrition, CSPEN)指南指出,术前筛查和评估明确为营养不良的患者,需要提供营养治疗。ESPEN指南建议6个月内体重丢失大于10%,血清白蛋白低于30g/L,主观整体评价法(subjective global assessment, SGA)评分C级或BMI小于18.5kg/m2的重度营养不良肿瘤患者,术前应给予7~14d的营养治疗。Wobith M和Weimann A提出胃癌患者术前给予免疫营养制剂5~7d可减少术后感染并发症,给予至少7d的ONS可缩短住院时间,并强调经口摄入不足目标量50%达到7d就应开始考虑ONS和管饲补充途径。Miyazaki Y等在日本的多中心Ⅲ期开放标签的随机对照试验中提出胃切除术后,要给予标准化的ONS达到200ml/d以上才会对患者术后1年的体重减少有积极保护作用。(2)肿瘤术后:吴国豪团队使用ONS的量约为500kcal/d,实际患者使用的平均量为每日370ml(约370kcal)可有效改善术后肿瘤患者的营养状况,维持肌肉量。Yamada T等报道一项关于高能量密度液体口服营养补充剂(100ml,400kcal,14g蛋白质)对胃全切和行Roux-en-Y肠道重建手术患者体重丢失的作用,ONS 组体重丢失率和瘦体重丢失率均有改善,但高能量密度的ONS在胃全切患者使用中因口味不耐受的中断率较高,因此不作为常规推荐。李庭等对ω-3多不饱和脂肪酸在肿瘤恶液质患者ONS中的作用进行了系统评价和meta分析,发现ω-3多不饱和脂肪酸强化的ONS可增加体重和改善生活质量,但不能改善患者去脂体重和延长生存时间。Lam CN等2021年更新的一项包含31项研究的meta分析却得出相反的结论,研究指出ω-3强化的ONS不能改变患者体重、肌肉量、生活质量,但能减少化疗引起的周围神经病变。Bumrungpert A等对静脉化疗患者使用乳清蛋白、锌、硒的ONS(分离乳清蛋白40g、锌2.64mg、硒0.76mg)进行随机对照安慰剂试验,试验组的清蛋白、免疫球蛋白G水平显著升高,而安慰剂对照组的谷胱甘肽水平显著下降,两组患者的SGA评分也有显著性差异。所有存在营养风险和/或营养不良诊断的肿瘤确诊患者,特别是肿瘤围手术期、放疗、化疗后体重丢失、虚弱、食欲缺乏、拒绝障碍等患者,更应在营养治疗中优先考虑规律的营养咨询和ONS。在外科大手术尤其是腹部大手术、高剂量放疗、高剂量化疗前,即使患者无营养不良,也可实施营养预康复,进行储备性医学营养治疗。终末期肿瘤患者,应优先充分考虑患者营养治疗的舒适度、患者自身的需求并充分结合家属的诉求,寻找对患者体验感最舒适、最容易接受的治疗途径,特别是经口进食或ONS时要充分考虑适口性和消化道的接受程度。中国抗癌协会肿瘤营养专业委员会制订了3顿正餐加3次ONS的3+3模式,建议一日3餐之间和晚餐后加用ONS,研究发现3+3模式可以显著提高患者的依从性和营养达标率(图2)。Plank LD等研究营养时相学发现,在能量及蛋白质相同时,夜间ONS比白天ONS更加有利于纠正营养不良。
1、存在营养风险或营养不良的胃肠道肿瘤患者术前5~7d应给予ONS,术后ONS结合运动锻炼对肿瘤患者的肌肉减少症有改善作用。2、胃肠道肿瘤手术患者术前ONS剂量不低于200~400ml/d。3、ω-3多不饱和脂肪酸强化的ONS不能改变患者体重、肌肉量、生活质量,但能减少化疗引起的周围神经病变。4、乳清蛋白质强化的ONS可改善肿瘤化疗清蛋白和免疫球蛋白水平,改善营养状况评分。5、终末期肿瘤的营养治疗,应优先充分考虑患者舒适度、患者自身需求并充分结合家属诉求,特别对经口进食或ONS充分考虑适口性和消化道接受程度。ONS是临床最为常见的肠内营养治疗手段,对明确存在营养风险/营养不良诊断的患者,根据中国抗癌协会肿瘤营养专业委员会制订的《五阶梯营养治疗原则》首先选择营养教育,然后再考虑口服营养补充等。肿瘤患者、任何转移性肿瘤患者可在肿瘤确诊时经验性早期启动医学营养。强化咨询联合ONS对患者疗效更确切。荷瘤患者优先选择肿瘤特殊型营养制剂,术前5~7d给予ONS可预防切口感染等并发症,强化特殊营养素如HMB可增加肌肉力量,乳清蛋白质强化可改善免疫功能,ω-3多不饱和脂肪酸强化可减少化疗引起的周围神经病变。ONS不能延长患者的生存时间,改善生活质量、体重、肌肉量。终末期肿瘤患者,应优先充分考虑患者营养治疗的舒适度、患者自身需求并充分结合家属诉求,特别对经口进食或ONS要充分考虑适口性和消化道接受程度。







